Kanser tədqiqatı: DNT ardıcıllığı və Genomik analiz metodları
2012-ci ildən 2023-cü ilə qədər Cənubi Koreyanın Samsung Tibb Mərkəzi və Seul Müqəddəs Məryəm Xəstəxanasında aparılan genişmiqyaslı kanser tədqiqatı xərçəngin molekulyar xüsusiyyətlərini dərinlemesine öyrənib. Tədqiqat, həm proqressiv, həm də retrospektiv olaraq toplanmış kohortlardan iştirakçıları əhatə edib. Retrospektiv hallar diaqnozdan qısa müddət sonra, əsasən cərrahi müdaxilə zamanı əldə edilmiş arxivləşdirilmiş ilkin şiş və uyğun normal qan nümunələrinin mövcudluğuna əsasən seçilib. Bu yanaşma, xəstəliyin mərhələsindən və ya sağ qalma statusundan asılı olmayaraq, geniş spektrli məlumatların toplanmasına imkan verib. Tədqiqat hər iki müəssisənin Etika Komitələri tərəfindən təsdiqlənərək, Helsinki Bəyannaməsinə və Yaxşı Klinik Təcrübə təlimatlarına uyğun şəkildə həyata keçirilib. Bütün proqressiv iştirakçılardan məlumatların istifadəsi və nəşri üçün yazılı məlumatlı razılıq alınıb. Retrospektiv hallarda isə, müvafiq icazə ilə məlumatlı razılıqdan imtina edilib. Bəzi iştirakçılar NCT03131089 və NCT06334471 klinik sınaqları çərçivəsində alt-tədqiqat komponentləri kimi cəlb ediliblər.
Nümunələrin hazırlanması və DNT ardıcıllığı
Tədqiqatda CancerVision platformasından istifadə olunaraq bütün genomik analiz həyata keçirilib. Rutin klinik qulluq çərçivəsində, cərrahiyyə və ya biopsiya yolu ilə əldə edilən şiş nümunələri təzə dondurulmuş toxuma şəklində saxlanılıb. Biopsiya nümunələrindən əvvəlcə rutin patologiya üçün, sonra isə kanser üçün ən azı bir əlavə nümunə götürülüb. Uyğun normal nümunələr üçün isə periferik qan istifadə edilib. DNK-nın çıxarılması və kitabxana hazırlanması CLIA sertifikatlı Inocras laboratoriyasında həyata keçirilib. DNK çıxarılması üçün Allprep DNA/RNA Mini Kit, kitabxana hazırlanması üçün isə TruSeq DNA PCR-Free dəstləri tətbiq olunub. DNT ardıcıllığı Illumina NovaSeq6000 platformasında, şiş nümunələri üçün orta hesabla 40x, qan nümunələri üçün isə 20x dərinliklə aparılıb.
Bütün transkriptom ardıcıllığı üçün isə, AllPrep DNA/RNA Mini Kit istifadə edilərək ümumi RNT çıxarılıb. RNT-nin miqdarı və keyfiyyəti Qubit Fluorometer və TapeStation RNA ScreenTape vasitəsilə qiymətləndirilib. RNT ardıcıllığı analizləri həm kodlaşdıran, həm də kodlaşdırmayan RNT-ləri, o cümlədən uzun intergenik kodlaşdırmayan RNT (lincRNA), kiçik nüvə RNT (snRNA) və kiçik nüvəcik RNT (snoRNA) aşkarlamağa imkan verib. RNT ardıcıllığı kitabxanaları KAPA RNA HyperPrep Kit ilə hazırlanaraq, Illumina NovaSeq 6000 platformasında sekvensiya edilib.
Genomik analizin tətbiqi
Genomik analiz və şərhlər Inocras-ın CancerVision platforması vasitəsilə aparılıb. Ardıcıllıq məlumatları GRCh38 insan referans genomuna bwa-mem alqoritmi ilə uyğunlaşdırılıb. Somatik SNV-lər və qısa indellər Mutect2 və Strelka2 proqramları ilə müəyyən edilib. Yüksək etibarlı somatik variantlar üçün bir sıra ciddi meyarlar tətbiq edilib: şişdə ≥2, normal nümunədə ≤1 variant oxunuşu, xəritələşdirmə keyfiyyəti ≥15 və şişdə variant allel tezliyi (VAF) ≤5%.
Şişin təmizliyi, ploidy və seqmentləşdirilmiş CNV profilləri Sequenza ilə, somatik struktur variasiyalar isə Delly ilə identifikasiya edilib. GISTIC alqoritmi rekurrent olaraq amplifikasiya edilmiş və ya silinmiş genomik bölgələri müəyyən etmək üçün istifadə olunub. Ecdna amplikonları AmpliconArchitect ilə aşkar edilib. Variantların annotasiyası Ensembl Variant Effect Predictor (VEP) ilə aparılıb. Bütün variantlar, həm irsi, həm də somatik, Inocras-ın xüsusi genom brauzerində ciddi şəkildə əl ilə nəzərdən keçirilib.
Protein-kodlaşdırıcı sürücü genlərin müəyyən edilməsi
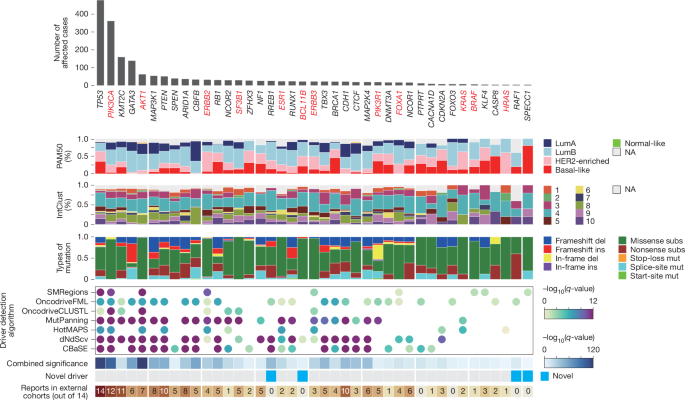
Protein-kodlaşdırıcı sürücü genlər IntOGen pipeline (v.2023) istifadə edilərək müəyyən edilib. Bu sistem yeddi müstəqil sürücü gen müəyyənləşdirmə metodunu birləşdirir. Bu metodlar kanser genomlarındakı somatik mutasiyaların selektiv üstünlüyünü qiymətləndirir. Konsensus sürücü genlərini müəyyən etmək üçün, hər bir metoddan ən yaxşı 100 gen seçilərək COSMIC Kanser Geni Siyahısındakı (CGC) məlum sürücülərlə müqayisə edilib. Schulze səsvermə metodu ilə yekun konsensus sıralaması əldə olunub. Namizəd sürücülər dN/dS nisbətlərinə əsasən onkogenlər (missense mutasiyaların nonsense mutasiyalardan üstün olduğu) və ya şiş suppressor genləri (nonsense mutasiyaların missense mutasiyalardan üstün olduğu) kimi təsnif edilib. Yüksək etibarlılığı təmin etmək üçün, tanınmış artefaktlar və ədəbiyyatla uyğun gəlməyən genlər (məsələn, PABPC1, JAK1) süzgəcdən keçirilib.
Mutasiya imzalarının analizi
Mutasiya imzalarının hər bir nümunədəki mutasiya spektrinə verdiyi töhfələr qiymətləndirilib. Bu analizdə müşahidə olunan mutasiya tiplərinin sayına və əvvəlcədən təyin edilmiş mutasiya imza matrisinə əsaslanan məhdudiyyətli optimallaşdırma problemi həll edilib. R paketi pracma istifadə olunaraq bu məsələ həll edilib. Bu metod SigProfiler və SignatureAnalyzer kimi alqoritmlərə oxşar performans göstərib. Dəri kanserlərində əvvəlcədən müəyyən edilmiş 16 konsensus mutasiya imzası (COSMIC SBS1, SBS2, SBS3, SBS5, SBS8, SBS13, SBS17a, SBS17b, SBS18, ID1, ID2, ID3, ID5, ID6, ID8 və ID9) tətbiq edilib. Bəzi nümunələrdə, kosinus bənzərliyi 0.90-dan aşağı olduqda, imzaların dəqiqliyini artırmaq üçün əlavə COSMIC imzaları (məsələn, SBS9, SBS10a, SBS10b, SBS31, SBS21, SBS44, SBS84, SBS34, SBS41, ID4 və ID11) daxil edilib.
HRD və MSI-ın qiymətləndirilməsi
Homolog Rekombinasiya Çatışmazlığını (HRD) qiymətləndirmək üçün xüsusi alqoritm tətbiq edilib. Bu alqoritm nöqtə mutasiyalarının mutasiya imzaları (SBS3 və SBS8), indel imzası (ID6), genomik yenidən düzəliş imzaları (RS3 və RS5), mikrohomologiya ilə müşayiət olunan delesiyalar və CNV-lər kimi HRD ilə əlaqəli xüsusiyyətləri birləşdirir. Mikrosatellit Qeyri-sabitliyinin (MSI) kəmiyyət qiymətləndirilməsi üçün MSIsensor proqramının nəticəsi və MSI ilə əlaqəli mutasiya imzalarının (SBS6, SBS15, SBS20, SBS21, SBS26, SBS30 və SBS44) nisbəti nəzərə alınıb.
Mutasiya kopiya nömrələri və amplifikasiya hadisələrinin zamanlaması
Mutasiya kopiya nömrəsi (nmut) əvvəlcədən təsvir edilmiş bir düsturla hesablanıb. Bu düstur variant allel fraksiyası (fs), şişin hüceyrəliyi (ρ), şiş və normal hüceyrələrdəki mütləq kopiya nömrələrini (ntlocus və nnlocus) əhatə edir. Bir mutasiya, nmut şişin əsas kopiya nömrəsinin 0.75 mislindən böyük olduqda amplifikasiya öncəsi hadisə kimi təsnif edilib. Əks halda, amplifikasiya sonrası və ya kiçik allel mutasiyaları kimi qiymətləndirilib.
Xərçəngdə DNT qazanclarının molekulyar zamanlaması
Xromosom seqmenti qazanıldığında, o, həmin seqmentdə o vaxta qədər əldə edilmiş bütün somatik mutasiyaları birlikdə amplifikasiya edir. Bu, genomik qazancların nisbi zamanlamasını bu mutasiyaların tezliklərini müqayisə etməklə müəyyən etməyə imkan verir. Fərdi şişlər daxilində hadisələrin nisbi zamanlamasını qiymətləndirmək üçün hər bir kopiya qazanımı üçün nisbi zamanlama ölçüsü (π) istifadə edilib. Bu ölçü, hadisədən əvvəl baş verən mutasiyaların DNT-nin vahid uzunluğuna düşən nisbətini ifadə edir. Hipermutator fenotipə (məsələn, APOBEC mutagenezi, MSI və HRD) səbəb olan mutasiya proseslərinin təsirini aradan qaldırmaq üçün, hər bir amplifikasiya edilmiş seqmentdəki mutasiyaların sayı SBS1 və SBS5-in saat kimi təbiəti nəzərə alınaraq tənzimlənib.
Kanser subtypeslərinin müəyyən edilməsi
Dəri kanser nümunələri PAM50 gen ifadə profilləşdirmə metodu ilə daxili alt tiplərə təsnif edilib. Gen ifadə məlumatları yükləndikdən sonra, genefu paketindən molecular.subtyping funksiyası istifadə edilərək nümunələr beş kateqoriyaya ayrılıb: luminal A, luminal B, HER2-zənginləşdirilmiş, bazal-tip və normal-tip. Şiş nümunələrinin inteqrativ klasterlərə (IntClust) təsnifatı üçün ic10 R paketi tətbiq olunub. Bu metod METABRIC kohortundan yaranıb və on kanser molekulyar alt tipini müəyyənləşdirmək üçün gen ifadəsi və seqmentləşdirilmiş kopiya nömrəsi variasiya məlumatlarını inteqrasiya edir.
Fokal amplifikasiya olunmuş genomik bölgələrin qiymətləndirilməsi
Bütün genomda fokal amplifikasiyaların mənzərəsini qurmaq üçün hər 5 Meqabazlıq (Mb) pəncərə üçün F-skoru hesablanıb. Hər nümunə üçün hər pəncərədə ən yüksək kopiya nömrəsinə malik seqment müəyyən edilib və bu kopiya nömrəsinin seqmentin eninə nisbəti hesablanıb. Daha sonra bu nisbətlər bütün nümunələr üzrə cəmlənərək F-skoru müəyyən edilib və bütün genom boyunca təsvir edilib.
Sağ qalma analizi
Sağ qalma analizlərində istifadə olunan bütün şiş nümunələri hədəf terapiyaların başlanmasından əvvəl toplanıb ki, nəticələr müalicənin səbəb olduğu genomik dəyişikliklərdən təsirlənməsin. Sağ qalma analizləri Kaplan-Meier metodu ilə aparılıb və qruplar arasındakı fərqlər log-rank testi ilə müqayisə edilib. Proqressiyasız sağ qalma (PFS) müalicənin başlanğıcından xəstəliyin proqressiyasına və ya istənilən səbəbdən ölümə qədərki vaxt kimi müəyyən edilib. Ümumi sağ qalma (OS) diaqnozdan istənilən səbəbdən ölümə qədərki vaxt kimi ölçülüb. Xəstəliksiz sağ qalma isə adjuvant müalicənin başlanğıcından ilk sənədləşdirilmiş residivə və ya istənilən səbəbdən ölümə qədərki vaxt kimi təyin edilib. Bütün sağ qalma analizlərində həm kanser ilə əlaqəli, həm də əlaqəsiz ölümlər hadisə kimi qəbul edilib. Spesifik dəyişənlər və sağ qalma nəticələri arasındakı əlaqəni qiymətləndirmək üçün Cox proporsional risk reqressiya modeli tətbiq edilib.
Statistika və təkrar istehsal olunma
Bütün statistik testlər və metodlar fiqur legendalarında təsvir edilib. Bütün məlumatların işlənməsi və ikinci dərəcəli hesablama analizləri üçün R (v.3.4.0) proqram təminatından istifadə edilib.

Oxucu Şərhləri
Hələlik heç bir şərh yazılmayıb. İlk şərhi siz yazın!
Şərh Yaz